THÔNG TIN THUỐC MỚI ĐƯỢC FDA CHẤP THUẬN
Người biên soạn: ThS DS Nguyễn Việt Nhựt Quang
HOẠT CHẤT: capivasertib
BIỆT DƯỢC: Truqap
NHÀ SẢN XUẤT: AstraZeneca Pharmaceuticals LP
DẠNG BÀO CHẾ: Dạng viên nén ở 2 hàm lượng:
-
- Viên nén 160 mg: Viên nén màu be, bao film, hình tròn, có dập chìm chữ 'CAV' phía trên '160' ở một mặt và phẳng ở mặt còn lại.
-
- Viên nén 200 mg: Viên nén màu be, bao film, hình dạng hình nón, có dập chìm chữ 'CAV 200' ở một mặt và phẳng ở mặt còn lại.
.png)
.png)
THÀNH PHẦN:
Hoạt chất: capivasertib
Tá dược
CƠ CHẾ TÁC DỤNG
Capivasertib là một chất ức chế của cả 3 dạng isoform của kinase serine/threonine AKT (AKT1, AKT2 và AKT3) và ức chế quá trình phosphorylation của các chất xúc tác AKT. Sự kích hoạt của AKT trong các khối u là kết quả của quá trình kích hoạt các đường tín hiệu, các đột biến trong AKT1, mất chức năng của phosphatase và tensin homolog (PTEN) và các đột biến trong phân đơn vị alpha của phosphatidylinositol 3-kinase (PIK3CA). Trong thử nghiệm in vitro, capivasertib đã làm giảm sự phát triển của dòng tế bào ung thư vú bao gồm cả những dòng tế bào có đột biến PIK3CA hoặc AKT1 hoặc biến đổi PTEN có liên quan. Trong thử nghiệm in vivo, capivasertib đơn độc và kết hợp với fulvestrant đã ức chế sự phát triển khối u trên mô hình xenograft chuột bao gồm các mô hình ung thư vú có kích hoạt receptor estrogen và có các biến đổi trong PIK3CA, AKT1 và PTEN.
CHỈ ĐỊNH
TRUQAP, kết hợp với fulvestrant, được chỉ định để điều trị bệnh nhân người lớn mắc bệnh ung thư vú cục bộ tiến triển hoặc di căn, có receptor hormone (HR) dương tính, không có yếu tố tăng trưởng nhân tử HER2 (HER2)-âm tính, với một hoặc nhiều biến đổi PIK3CA/AKT1/PTEN được phát hiện bằng cách sử dụng một bài kiểm tra được FDA chấp thuận, sau khi tiến triển sau ít nhất một liệu pháp endocrine trong môi trường di căn hoặc tái phát trong khoảng thời gian 12 tháng sau khi hoàn thành liệu pháp bổ trợ.
LIỀU DÙNG
Liều khuyến nghị của TRUQAP, kết hợp với fulvestrant, là 400 mg uống hai lần mỗi ngày (khoảng cách khoảng 12 giờ) có hoặc không có thực phẩm, trong 4 ngày sau đó nghỉ 3 ngày. Tiếp tục sử dụng TRUQAP cho đến khi bệnh tiến triển hoặc gặp tác dụng phụ không chấp nhận được.
Liều trình dùng TRUQAP cho mỗi tuần được cung cấp trong Bảng 1.
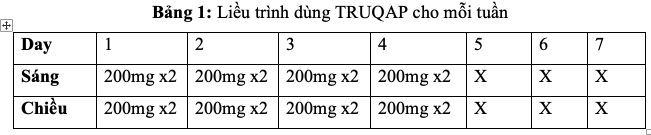
X: không dùng thuốc ở ngày 5, 6, 7
.png)
CÁCH DÙNG:
Uống viên TRUQAP nguyên vẹn. Không nhai, nghiền, hoặc chia nhỏ viên trước khi nuốt. Không dùng viên đã bị vỡ, nứt, hoặc không nguyên vẹn.
Nếu bệnh nhân bỏ sót một liều trong vòng 4 giờ kể từ giờ dự kiến, hướng dẫn bệnh nhân uống liều đã bỏ sót. Nếu bệnh nhân bỏ sót một liều quá 4 giờ kể từ giờ dự kiến, hướng dẫn bệnh nhân bỏ qua liều đã bỏ sót và uống liều tiếp theo vào giờ dự kiến thông thường.
Nếu bệnh nhân nôn sau khi dùng liều, hướng dẫn bệnh nhân không uống thêm liều và uống liều tiếp theo vào giờ dự kiến thông thường.
Đối với phụ nữ tiền mãn kinh và mãn kinh gần đây, tiêm một chất kích thích hormone tạo hormone luteinizing (LHRH) theo tiêu chuẩn thực hành lâm sàng hiện tại.
THẬN TRỌNG:
- Tăng đường huyết: Đánh giá mức độ đường huyết trước khi bắt đầu và định kỳ trong suốt quá trình điều trị. Ngừng, giảm liều hoặc chấm dứt việc sử dụng TRUQAP vĩnh viễn dựa trên mức độ nghiêm trọng.
- Tiêu chảy: TRUQAP gây ra tiêu chảy ở phần lớn bệnh nhân. Khuyến nghị bệnh nhân tăng cường uống nước, bắt đầu điều trị chống tiêu chảy và tham khảo ý kiến của nhà cung cấp dịch vụ y tế nếu tiêu chảy xảy ra trong quá trình sử dụng TRUQAP. Ngừng, giảm liều hoặc chấm dứt việc sử dụng TRUQAP vĩnh viễn dựa trên mức độ nghiêm trọng.
- Độc tính thai nhi: TRUQAP có thể gây hại cho thai nhi. Khuyến nghị bệnh nhân về nguy cơ tiềm ẩn cho thai nhi và sử dụng biện pháp tránh thai hiệu quả. Tham khảo Thông tin đầy đủ về cách sử dụng fulvestrant để biết thông tin về thai kỳ và phương pháp tránh thai.
TÁC DỤNG PHỤ:
Các phản ứng phụ phổ biến nhất (tỷ lệ ≥20%), bao gồm: tiêu chảy, các phản ứng da bất lợi, tăng đường huyết ngẫu nhiên, giảm số lượng lymphocytes, giảm hemoglobin, tăng đường huyết nhanh, buồn nôn, mệt mỏi, giảm số lượng leukocytes, tăng triglycerides, giảm số lượng neutrophils, tăng creatinine, nôn mửa và viêm loét miệng.
CHỐNG CHỈ ĐỊNH
TRUQAP bị chống chỉ định đối với bệnh nhân có mức độ quá mẫn cảm nghiêm trọng đối với bất kỳ thành phần nào của thuốc.
Nguồn: Novel Drug Approvals for 2024 | FDA
Breast Cancer Treatment | TRUQAP™ (capivasertib) Tablets




